حصول اطمينان از اين كه دارو به بافت يا بخش مورد نظر بدن بيمار هدايت شود و همچنين اطمينان از ميزان داروي استفاده شده ، دو نمونه از مهم ترين مسائل پزشكي نوين هستند. اين امر به طور خاص براي درمان سرطان اهميت دارد. چون داروهاي شيمي درماني براي سلولهاي عادي و سرطاني مانند سم عمل ميكنند.
به خاطر ناسازگاري برخي مواد با بدن و دفع سريع آنها توسط سامانه ايمني بدن ، داروها به طـور مـوقـت در داخل يك ساختار هماهنگ با سامانه ايمني بدن قرار ميگيرند و در هنگام نياز در مـوضـع بـيـماري به سرعت از داخل آن آزاد ميشوند.
در دارورساني تمام تلاش محققان بر ساخت روباتهايي است كه در داخل بدن بتوانند وارد شوند. خود را به موضع مناسبي برسانند و سلول زيان بار را نابود كنند. آنها بايد كاري كنند كه اين روبـاتهـا بـا سـامـانه ايمني بدن ، امواج گرمايي اداره كننده گردش خون و تعادل بدن ، هماهنگ و سازگار باشند.

انتقال دارو از پوست
قـورت دادن يـك قـرص مـعـمـولا كار آساني است اما هنوز هم خيليها فراموش ميكنند كه داروهاي خود را به موقع و به اندازه مصرف كنند و مقدار دارو يا دز دارو در خون افت و خيز دارد. چسبهاي دارويي كه به پوست ميچسبند ، از اين مشكلات جلوگيري ميكنند. اين چسبها در سال 1990 براي ترك اعتياد مورد استقبال قرار گرفت. مجموعه اي از اين چسبها چند هفته كه مورد استفاده قرار ميگرفت ، مقدار نيكوتين بدن را به تدريج كاهش ميداد و با اين كار فرد به مرور اعــتــيـاد خــود را از دســت مـيداد. امــروزه چسـبهاي پوستي براي انتقال استروژن براي درمـان بيمـاريهـاي هـورمـون ، نيتـروگليسيـرين براي گلودرد ، اسكوپولامين براي بيماريهاي حركتي و دريازدگي ، فنتانيل براي كنترل درد و كلونيدين براي فشار خون بالا مورد استفاده قرار ميگيرد. سالها تحقيقات به بررسي احتمالي و حد تحقق دارورساني تراپوستي (دارورساني از پوست) اختصاص يافته است. اولين مدل موفق براي انتقال تراپوستي در سال 1979 ايجاد شد.
انواع چسبهای پوستی
برچسبهای ميكروسوزنی: اين برچسبها دارو را در يك مايع يا پليمر نگهدارنده ذخيره ميكنند.
چسب تک لايه: يك چسب پليمري كه به پوست ميچسبد و دارو را دربر مي گيرد.
چسب چند لايه: چسب چندلايه غشايي دارد كه نرخ تغذيه دارو را به ويژه داروهايي كه بايد خيلي كند به پوست تغذيه شوند.
مسأله اصلي در چسبهاي درماني ، انتقال آسان و مؤثر دارو از طريق دو سد اصلي پوست يعني استراتوم كورنئوم و اپيدرميس است كه استراتوم كورنئوم اهميت بيشتري دارد. استراتوم كورنئوم 10 تا 15 ميكرومتر ، اپيدرميس 10 تا 50 ميكرومتر و لايه درميس 2 تا 3 ميليمتر ضخامت دارد. معمولا دارو يا ناقل انتقال تراپوستي نميتواند به آساني از استراتوم كورنئوم عبور كند. فناوري نانو نقش برجسته اي در اين موارد دارد. داروهاي نانومتري ، ميتوانند به صورت مستقيم و مؤثر به اپيدرميس انتقال داده شوند. اندازه كوچكتر داروها ، نفوذپذيري را آسان ميكند.
ردياب نانو دارو
طرح فيلتر غيرخطي براي رديابي نانو دارو در بدن حيوانات كه در مركز رشد دانشگاه علوم پزشكي اجرايي شد ، به ثبت خارج رسيد.
اين طرح با عنوان "فيلتر غيرخطي براي تصويربرداري پزشكي" با هدف ارتقاي سطح كيفي دستگاههاي ساخته شده در عرصه تصويربرداري پزشكي هسته اي در مركز رشد مركز تحقيقات تجهيزات پزشكي دانشگاه تهران اجرايي شد.
اين طرح در واقع تهيه الگوريتمي براي پردازش سيگنالهاي هسته اي است و عموماً تجهيزاتي مانند SPECT و PET كه اين الگوريتم در آنها كاربرد دارد از دستگاههاي با فناوري بالا محسوب ميشوند. اين دستگاهها در مطالعات دارويي براي رهگيري نانو داروها در بدن حيوانات آزمايشگاهي كاربرد دارد.
تصـويـربـرداري از حيـوانـات كـوچـك شـاخه جديدي از تصويربرداري است كه با استفاده از دستگاه اسپكت حيواني HiReSPECT امكانپذير خـواهـد بـود. عملكرد اين دستگاه بدين ترتيب است كه راديو دارو يا نانو داروي مورد نظر در رگ موش تزريق ميشود و سپس دستگاه با سيستم آشكارسازي خود تعدادي تصوير دو بعدي از زواياي مختلف در بازه 360 درجه از موش تهيه ميكند. سپس يك نرمافزار كامپيوتري با استفاده از دادههاي بهدست آمده ، يك تصوير سهبعدي از نـحــوه و مـيــزان پـراكنـدگـي دارو در مـوش را بازسازي خواهد كرد.
ايـن دسـتـگـاه ، مـخـصوص تصويربرداري از حيوانات كوچك مانند موش و خرگوش است. زمـــانـــي كـــه دارويـــي تـــولــيــد مــيشــود ، قـبــل از كاربردهاي كلينيكي بايد مراحل پيش كلينيكي و تست بر روي حيوانات آزمايشگاهي را طي كند. بـراي ايـن مـنـظور نياز به سيستم تصويربرداري است كه كيفيت بالايي داشته باشد.
از اين رو دستگاهي كه براي تصويربرداري از حيوان كوچك مورد استفاده قرار ميگيرد ، بايد داراي قـابـلـيـت بـسـيار بالايي در تفكيك مكاني باشد.
درواقع دستگاه تصوير برداري اسپكت جهت تـصـويربرداري از مراحل درمان و تزريق راديو دارو به بدن حيوانات زنده ، جهت درمان و توليد داروهاي جديد مورد استفاده قرار ميگيرد و در تحقيقات بنيادي در زمينه توليد راديو داروهاي مـخـتـلــف ، مـحـصــولــي اسـتـراتـژيـك بـه حـسـاب ميآيد.
نانو داروی ترميمكننده زخم
اين نوآوري يك پوششدهنده پوستي است كــه شــامـل نـانـوذرات پكتيـن حـاوي مـواد فعـال ترميمكننده زخم و همچنين مواد آنتيباكتريال است. اين پوششدهنده زخم از پليمرهايي با بار مثبت يا منفي تشكيل شده است كه سطح زخم را پـوشـانـده و از آن مـحافظت ميكند. آزادسازي مواد فعال ترميمكننده زخم و مواد ضد ميكروبي از نــانــوذرات بـه صـورت كـنـتـرل شـده صـورت ميگيرد و باعث تسريع در بهبود زخم ميشود.
در اين مطالعه روشي بسيار ساده براي تهيه نانو ذرات پكتين حاوي مواد فعال ترميمكننده زخم بـه كـار گـرفتـه شـده است. اين روش بر خلاف برخي روشهاي تهيه نانو ذرات بدون استفاده از حلالهاي آلي يا روشهايي مانند سونيكاسيون يا هموژنايزر كه باعث تخريب برخي مواد فعال مثل پپتيدها و پروتئينها ميشود ، نانوذراتي با اندازه مناسب تهيه ميكند. رهايش كنترل شده مواد فعال از اين محصول ، مزيتي مهم نسبت به ساير محصولاتي است كه رهايش كنترل شده ندارند. با توجه به اينكه مواد فعال در اين مطالعه درون نانو ذرات قرار گرفتهاند ، رهايش مواد فعال به صورت كنترل شده و تقريباً به صورت درجه صفر صورت ميگيرد.
ايـن محصـول به صورت ليوفيليزه (خشك كردن در خلاء) تهيه ميشود ، بنابراين مشكـل عـدم پـايـداري و تخـريب سريع به خصوص براي پپتيدها و پروتئينها كه در محصولات ديگر وجود دارد ، ديده نميشود. استفاده از اين محصول بسيار راحت بوده و حتي ميتواند توسط خود بيمار نيز مورد استفاده قرار گيرد و منجر به كاهش هزينههاي پرستاري و بستري بيمار شود. همچنين تهيه اين محصول بسيار راحت و كم هزينه است. اين محصول ميتواند به راحتي توسط فرايند فيلتراسيون استريل شود و نسبت به ساير محصولاتي كه با روشهاي ديگر استريل ميشوند ، هزينه كمتري براي توليد نياز دارد.
نانو كپسولهای گنبدی در دارو رسانی
محققان در سالهاي اخير با اين چالش دست به گريبان بودهاند كه بتوانند تأثير عوامل درماني را از طريق رسانش آنها به سلولهاي خاص درون بدن افزايش داده و در عين حال تأثير منفي آنها را روي سلولهاي سالم به كمترين مقدار خود برسانند.
در اين زمينه استفاده از روشهاي جديدي كه از نانو مواد مهندسي شده براي انتقال داروهـا و رسـانـش مستقيـم آنهـا به سلولها بهره ميبرند ، نويد بخش بوده است. با وجودي كه سامانههاي رسانشي مختلفي از اين دست براي كاربردهاي باليني مورد تأييد قـرار گرفتهاند ، اما مشكل تمام اين سامانهها محدوديت اندازه و ناكارآمدي آنها در هـدفگيـري دقيـق بـافـتهـا اسـت. نانو ذرات گنبدي در سيتوپلاسم تمام سلولهاي پستانداران يافت شده و يكي از بزرگترين كمپلكسهاي ريبو نوكلئو پروتييني شناخته شده در مقياس زير 100 نانومتر به شمار ميرود. اين نانوذرات بشكهاي شكل با دارا بودن فضاي داخلي بزرگ و توخالي ، گزينههاي مناسبي براي طراحي حاملهاي رسانش دارو به شمار ميروند. گنبدهاي نو تركيب ، غير ايمنيزا بوده و متحمل تغييرات مهندسي زيادي شدهاند كه از آن جمله ميتوان به هدفگيري گيرنده سطح سلول و كپسوله كردن محدوده وسيعي از پروتيينها اشاره كرد.
حفره داخلي يك نانو ذره گنبدي آن قدر بزرگ است كه ميتواند صدها مولكول دارو را در خود جاي دهد. از سوي ديگر خود اين ذراتگنبدي به اندازه يك ميكروب هستند و بنابراين ميتوانند به راحتي همراه با محتواي خود وارد سلولهاي هدف شوند.
محققان با هدف ايجاد يك ذره گنبدي كه بتواند تركيبات درماني را در خود كپسوله كند ، راهكاري براي بستهبندي نانوذره ديگري به نام نانوديسك درون حفره داخلي ذره گنبـدي ارائه كردهاند. با كپسوله كردن نانو ديسكهاي حاوي دارو درون حفره ذره گنبدي ، اين نانو ديسكها و محتواي آنها از محيط بيروني محافظت ميشوند.
به علاوه ، با توجه به فضاي داخلي بزرگ ذره گنبدي ، ميتوان چندين نانو ديسك را درون آن كپسوله كرد كه اين كار غلظت موضعي داروي رها شده را افزايش داده و شانس درمان را افزايش ميدهد.
نانو تكنولوژی در انتقال دارو
فناوري نانو جنبههاي مختلف دنياي امروز را تحت تأثير خود قرار داده است. انتقال كنترل شده دارو به اندام هدف ، يكي از كاربردهاي مهم نانو فـنـــاوري اســت. مــيتــوان داروهــا را بــه كـمــك حاملهاي مختلف به اندام هدف رساند. استفاده از حاملهاي مختلف به عنوان ناقلهاي دارو در حـــال گـسـتــرش اســت. بــا روشهــاي مـعـمــول مصرف دارو ، نظير مصرف خوراكي و تزريقي ، دارو به سراسر بدن توزيع خواهد شد و تمام بدن تحت اثرات دارو قرار خواهد گرفت و عوارض جـانبـي دارو بـروز خـواهـد كـرد. بنـابـرايـن بـراي دسـتيـابـي بـه يـك اثـر خـاص ، نـيـاز بـه مصرف مـقــاديــر زيــادي از دارو اســت. بــا نــانـو فـنـاوري ميتوان به دارورساني هدفمند دست يافت و زمان ، مكان و سرعت آزادسازي دارو در بدن را كنترل نمود. سيستمهاي دارورساني جديد عوارض جانبي كمتر ، كارايي بيشتر و راحتي بيمار را به دنبال خواهند داشت.
نانو حاملها
حاملهاي مختلفي را ميتوان به عنوان ناقلهاي دارو در دارورساني مورد استفاده قرار داد. از آنجا كه دارو نقش درماني دارد ، بايد تا رسيدن به محل هدف در بدن محافظت شود و خواص شيميايي و بيولوژيكي خود را حفظ كند. برخي از داروها به شدت سمي بوده و ميتوانند سبب اثرات جانبي منفي شده و اگر حين آزاد شدن تخريب شوند ، اثر درماني آنها كاهش مييابد. به عنوان مثال ؛ در شيميدرماني داروهاي مصرفي تا حدي سـمـيانـد و افـزايـش مـقـدار آنها ميتواند اثر معكوس بگذارد و حتي به مرگ بيمار بيانجامد. به بيان ديگر ، اگر دارو بتواند مستقيماً به بافت هدف برسد و بر روي ساير قسمتهاي بدن تأثير نگذارد ، به مراتب مؤثرتر خواهد بود. در ادامه به برخي از حاملها دارو اشاره خواهد شد.
مايسل
يكي از حاملهايي كه به طور گسترده در دارورساني هدفمند به كار ميرود ، مايسل است. مايسلها از تجمع خودبخودي كوپليمرهاي آمفيفيلي در محلولهاي آبي به وجود ميآيند. شكل زیر ، مولكول آمفيفيلي را نشان ميدهد.
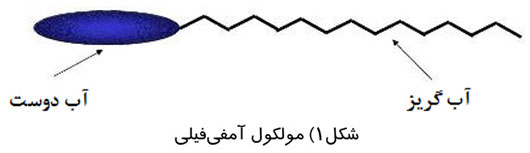
در حقيقت مايسلها داراي يك سر آبدوست (قطبي) و يك دم آبگريز (غيرقطبي) هستند كه در محلولهاي آبي به صورت خودبخودي تجمع مييابند. مايسلها در محيط آبي به نحوي جهتگيري ميكنند كه انتهاي آبگريز مايسلها از محلول آبي رانده شده و ايجاد يك فاز آبگريز داخلي يا هسته آبگريز كنند. در حالي كه انتهاي آبدوست مايسلها به طرف خارج ، يعني محلول آبي متمايل شده و يك تاج آبدوست را به وجود خواهند آورد. شكل زیر ، مايسل را نشان ميدهد.
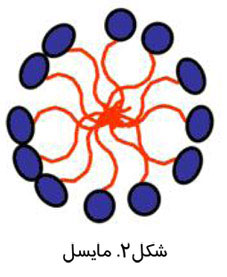
از اين رو ، ميتوان داروهاي آبگريز را با قرارگيري آنها در داخل مايسل به بافت هدف رساند و اثرات جانبي موجود را كاهش داد. ميتوان از مايسلها به عنوان ناقلها ، جهت رساندن دوز زياد داروهاي ضدسرطاني به تومورها و بافت هدف استفاده كرد و در عين حال اثرات جانبي آنها را به حداقل رساند. شكل زیر ، قرار گيري دارو در مايسل را نشان ميدهد.
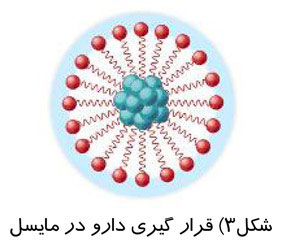
در نهايت محتويات مايسلها (داروي موجود در آن ها) تحت شرايط محيطي ويژه ، نظير دما ، نور UV ، اعمال ميدان مغناطيسي يا pH در بافت هدف آزاد خواهند شد. شكل و اندازه مايسل به طول زنجير پليمري ، نوع شاخه يا گروه متصل به زنجير ، نوع الكتروليت ، غلظت يوني ، استحكام يوني ، دماي موثر و pH بستگي دارد.
ليپوزمها
يكي ديگر از ناقلهايي كه به طور گسترده در دارورســانــي هـدفمنـد بـه كـار مـيرود ، ليپـوزوم اسـت. لـيـپـوزومهـا از نـوعي وزيكول با دو لايه لـيـپـيـدي ، مـشابه آنچه كه در غشاء سلولي ديده ميشود ، تشكيل شدهاند. شكل زیر يك ليپيد را نشان ميدهد.

به طور كلي ، دو لايه ليپيد در فاز آبي به گونهاي جـهـتگـيـري مـيكنند كه بخشي از فاز آبي در داخـل مـحـفـظه كروي محصور شود و ليپوزوم حـاصـل شـود. در ايـن مـيـان ، لـيپيدها گروهي از تـركـيـبـات شـيـمـيـايـي با زنجيره آلكيلي غيرقابل انـحـلال در آب و گـروه قـطـبـي مـحلول در آب هستند. بنابراين ، بخشي از اين مولكول آبگريز و بخش ديگر آبدوست است كه به مولكولي با چـنـيـن خـاصـيـت دوگـانـه ، مـولـكـول آمـفيفيلي ميگويند. به شکل زیر توجه کنید.
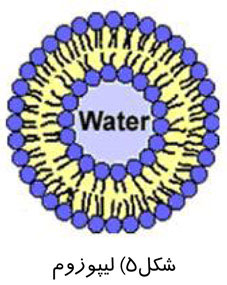
بــه طــور كـلــي لـيـپــوزومهـا تـوانـايـي رسـانـدن داروهـاي آبگـريـز ، آبدوسـت و آمفـيفيلـي (دوگانهدوست) را دارند. در حقيقت ، داروهـاي آبگـريـز در بخش غيرقطبي ليپوزوم قرار ميگيرند. حال آن كه داروهاي آبدوسـت در فـاز آب داخلـي ليپـوزوم قـرار خـواهند گرفت و داروهاي آمفي فيلي (دوگانه دوست) در حد فاصل بخش آب داخلي و بخش آبگريز قرار خواهند گرفت.
نانو ذرات
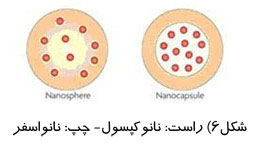
نــاقـل ديگـري كـه در دارورسـانـي هـدفمنـد كـاربـرد فـراوان دارد ، نـانـو ذرات شـامـل نانوكپسول و نانواسفر است. اين ناقلها قادر هستند كه دارو را جذب و كپسوله كرده و به ايـن تـرتـيـب دارو را عـلـيه تخريب آنزيمي و شيميايي محافظت نمايند. نانوكپسولها سيستمهاي وزيكولي هستند كه دارو را در حفرهاي محصور كرده و با يك غشاء پليمري احاطه ميكنند. در حالي كه در نانواسفرها ، دارو به صورت فيزيكي و يكنواخت در ماتريس پليمري پراكنده شده و در حقيقت دارو در درون نانواسفر به صورت پراكنده قرار گـرفـته است. در سالهاي اخير ، توجه قابل ملاحظهاي به نانوذرات پليمري زيست تخريب پذير ، به عنوان سيستمهاي مناسب براي دارورساني اختصاص يافته است. در شكل زیر ، دارو كه به صورت ذرات كروي قرمز رنگ نشان داده شده است ، در درون نانوكپسول و نانواسفر جاي گرفته است.
درختسانها
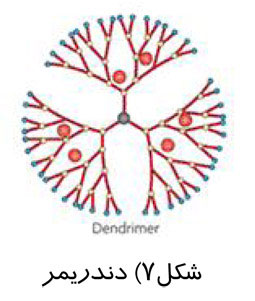
يكي ديگر از ناقلهاي مورد استفاده در دارورساني درختسان (دندريمر) است. دندريمرها، ماكرومولكول باريك، شاخه شاخه و متقارن هستند كه از يك هسته مركزي، واحدهاي منشعب شده به صورت درخت، و تعدادي گروه عاملي تشكيل شدهاند. هسته مركزي و واحدهاي داخلي آن، محيط داخل حفره براي قرارگيري دارو را به وجود ميآورند. با اتصال گروههاي عاملي هدفمند به سطح اين ماكرومولكولها، ميتوان حلاليت و رفتار شيميايي آنها را كنترل كرد. در شكل زیر ، دارو كه به صورت ذرات كروي قرمز رنگ نشان داده شده است ، در منافذ موجود در درون دندريمر جاي گرفته است.
كريستال مايع
ناقل ديگري كه در دارورساني هدفمند مورد استفاده قرار ميگيرد ، كريستالهاي مايع است. كريستالهاي مايع از لحاظ مولكولي بين حالت جامد و مايع قرار دارند ، در نتيجه همزمان خصوصيات جامد و مايع را دارا هستند. دارو ميتواند در بين مولكولهاي كريستال مايع كپسوله شده (قرار گيرد) و با تغيير فاز در نتيجه اعمال محرك ، دارو از سيستم آزاد خواهد شد.
نانوفناوري در دارورساني از جمله موارد رو به گسترش است. نانوذرات مختلف دارويي با تغيير ناقلها حاصل خواهند شد و امكان ايجاد تغيير در خصوصيات دارويي را به وجود خواهند آورد. به طور كلي ، بازار نانودارو رساني به طور شگفتانگيزي رو به جلو ميرود. از اين رو ، با استفاده از نانوفناوري ميتوان به دارورساني هدفمند دست يافت و با مصرف كمتر دوز دارو و كاهش اثرات جانبي ، راحتي بيمار را بدست آورد.
منبع: ماهنامه مهندسی پزشکی
نظرات شما عزیزان:

